2024 ASH | 与标准治疗相比,CARVYKTI® 显著提高了复发或难治性多发性骨髓瘤患者MRD阴性率
- 在CARTITUDE-4研究中,经过三年随访,89%的可评估患者在接受CARVYKTI®治疗后达到了微小残留病(MRD)阴性,其中多数患者在2个月内获得MRD阴性 。
- 近期报道的总生存期(OS)获益数据让 CARVYKTI® 成为首个且唯一一款在多发性骨髓瘤中相较于标准疗法能够显著延长OS的细胞疗法。
- 具有里程碑意义的3期研究CARTITUDE-4数据在第66届美国血液学会(ASH)年会暨展览会上作了口头报告。
南京2024年12月10日 /美通社/ -- 当地时间2024年12月9日,传奇生物(NASDAQ:LEGN)在美国新泽西州萨默塞特公布了3期研究CARTITUDE-4最新数据。该研究结果表明,在既往至少接受过一线治疗(包括一种蛋白酶体抑制剂 [PI] 和一种免疫调节剂 [IMiD])的复发或来那度胺耐药多发性骨髓瘤患者中,单次输注CARVYKTI®(西达基奥仑赛;cilta-cel)可显著提高微小残留病(MRD)阴性率,与标准治疗(泊马度胺、硼替佐米和地塞米松 [PVd] 或达雷妥尤单抗、泊马度胺和地塞米松 [DPd])相比疗效显著。[1] MRD阴性率是多发性骨髓瘤患者生存期延长的重要预后标志。[1] 这些结果强化了CARVYKTI®作为早期(二线)治疗的临床价值,并支持了其近期达到的相较于标准治疗的总生存期(OS)获益。[1] MRD阴性率的研究结果已在加利福尼亚州圣地亚哥举行的第66届美国血液学会(ASH)年会暨展览会上以口头报告的形式发表(摘要#1032)。[1]
美国梅奥诊所血液学和肿瘤学家Yi Lin博士*表示:"微小残留病(MRD)数据进一步强调了CARVYKTI®的治疗获益。这些新发现支持CARVYKTI®作为一种变革性治疗选择,能够显著改善患者无进展生存期(PFS)、OS和MRD阴性率。"
3期研究CARTITUDE-4评估了CARVYKTI®与 PVd 或 DPd 的标准疗法在既往接受过一至三线治疗且来那度胺耐药的复发或难治性多发性骨髓瘤成人患者中的疗效。研究进行了随机分组,208名患者接受CARVYKTI®治疗,211名患者接受标准治疗。
该研究评估了患者在10-5阈值下的MRD阴性率(cilta-cel组n=145;标准疗法组n=103)。在中位随访近三年(34个月)时,接受CARVYKTI®治疗的可评估患者MRD阴性率为89%,而标准疗法组为38%(P<0.0001)。此外,经CARVYKTI® 治疗的患者迅速达到了较高的总体MRD阴性率,在第56天时,69%的可评估患者已达到MRD阴性。在数据截止时,CARVYKTI®组中有52%的MRD可评估患者达到至少12个月的持续MRD阴性且完全缓解(≥CR),而标准治疗组仅为10%(P<0.0001)。对CARTITUDE-4和CARTITUDE-1研究(既往1-3线与3+线治疗)的事后比较表明,在治疗方案中更早使用CARVYKTI®治疗时,MRD阴性率、PFS 和 OS率更高。
传奇生物首席执行官黄颖博士表示:"最新的MRD数据展示了CARVYKTI®的优势,并进一步证明其作为多发性骨髓瘤患者的优先治疗选择。在努力改变癌症及其他领域治疗格局的过程中,我们为取得的进展感到自豪,并将继续努力改善那些与不治之症作斗争的患者的生活质量。"
来自CARTITUDE-4的数据支持了美国食品药品监督管理局(FDA)和欧盟委员会(EC)在今年早些时候批准CARVYKTI®用于治疗复发或难治性多发性骨髓瘤成人患者,这些患者既往至少接受过一线治疗,包括一种PI和IMiD且对来那度胺耐药。[1] CARVYKTI®是首个也是唯一一款获批用于治疗至少接受过一线治疗的多发性骨髓瘤患者的靶向BCMA的CAR-T细胞疗法。截至目前,我们已在全球五个国家推出了CARVYKTI®,治疗患者人数逾4500名。
- Cloudera 和 OCBC 荣获 2024 年金融科技创新奖
- 迪恩机床将亮相"CCMT 2024",展出高端机型及自动化解决方案
- 环保力量在民间,2024年广东珊瑚普查活动顺利启动
- 迈威生物靶向Nectin-4 ADC联合PD-1单抗一线治疗尿路上皮癌获CDE同意开展III期临床研究
- 融合巴伐利亚传统,TÜV南德2024年广州啤酒节圆满落幕
- Illusion Aligners凭借其在印度最大的Aligner取得创纪录的成就
- 以品质树标杆,视爵光旭荣获深圳标准认证
- 贝亲「仿生奶嘴3S模型」全球首发,揭秘"新生儿仿生奶嘴"黑科技
- Sirnaomics公布2023年全年业绩
- 万豪国际集团与德胧集团首批三个合作项目签约
- 花皙蔻牡丹化妆品全国销售额第一,问鼎牡丹化妆品赛道
- 软通动力携子公司鸿湖万联 共同揭幕鸿蒙生态创新中心
- 启明创投梁颕宇荣膺2024年福布斯Midas List全球最佳创投人
- 移远通信高性能5G-A模组RG650V-NA通过北美两大重要运营商认证
- 数智融合 驱动美好工业 美的工业技术携多款新品亮相2024工博会
- 立邦供应路特斯EMEYA繁花,以创新涂装科技为超跑披上优雅战衣
- 【引领绿色未来,中国生态畜牧产业网赋能可持续发展】
- 临商银行龙潭支行:员工家访暖人心 凝心聚力促发展
- 软通动力成功举办"软硬全栈,加速智能化赋能"分论坛
- Massimo Dutti旗舰店现已正式入驻京东
- GLP-1药物利拉鲁肽可能有助于预防痴呆
- SGS为HUAWEI xHUD颁发AR-HUD Premium Performance Mark
- 大连四季酒店Fresca甜品坊户外花园今日正式开启
- 华山A1000芯片助力智驾升级,东风奕派eπ007迎来重磅OTA
- Blue Owl Capital 聘请 Fidelity International 的 Johann Santer 领导亚太地区的私人财富业务
- 盛泰乐酒店集团成功举办京沪路演,深耕中国市场
- 华大电子获评2024年度优秀智能汽车信息安全解决方案提供商
- Steelhead液化天然气公司在韩国对Cedar液化天然气公司和三星重工提起专利侵权诉讼
- 李宁公司一行到访浙江体育职业技术学院,助力浙江健儿再续辉煌
- 第24届立嘉国际智能装备展览会5月13-16日在渝盛大开幕
推荐
-
 为何娃哈哈纯净水线上会卖断货?
随着网络上关于娃哈哈和农夫山泉之争的持续
财商
为何娃哈哈纯净水线上会卖断货?
随着网络上关于娃哈哈和农夫山泉之争的持续
财商
-
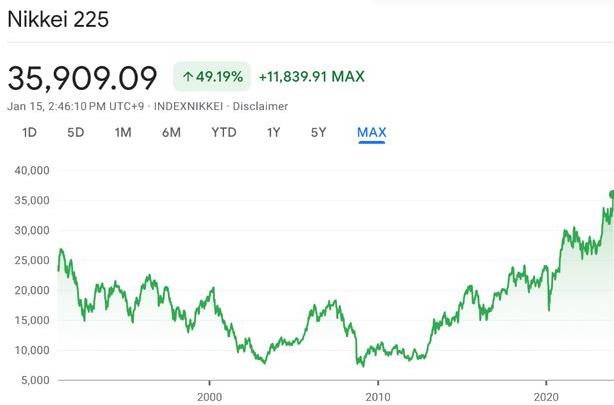 日股盘中再破34年新高,今年还涨得动吗?
今年日股开局强势,1月5日以来开启连涨行情,日
财商
日股盘中再破34年新高,今年还涨得动吗?
今年日股开局强势,1月5日以来开启连涨行情,日
财商
-
 广东省药监局调研恒昌医药集团,聚焦药品流通产业高质量发展
日前,广东省药品监督管理局党组成员、副
财商
广东省药监局调研恒昌医药集团,聚焦药品流通产业高质量发展
日前,广东省药品监督管理局党组成员、副
财商
-
 娃哈哈这艘商业巨舰将驶向何方,我们试目以待
2月25日,娃哈哈集团在官网发布讣告,娃哈哈创
财商
娃哈哈这艘商业巨舰将驶向何方,我们试目以待
2月25日,娃哈哈集团在官网发布讣告,娃哈哈创
财商
-
 我们时常把创业想得太过简单,认为获得成功轻而易举
我们时常把创业想得太过简单,认为获得成功
财商
我们时常把创业想得太过简单,认为获得成功轻而易举
我们时常把创业想得太过简单,认为获得成功
财商
-
 春节将至,抢票再次成为广大网友关注的热门话题
春节将至,抢票再次成为广大网友关注的热门话
财商
春节将至,抢票再次成为广大网友关注的热门话题
春节将至,抢票再次成为广大网友关注的热门话
财商
-
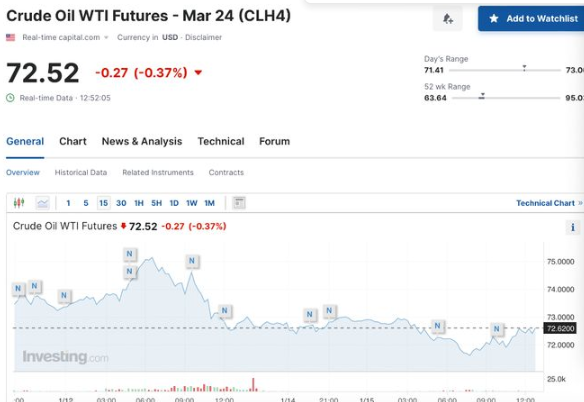 供应“安全感”超过红海“危机感”?欧洲天然气价格大跌
虽然冬季极寒天气来临,而且卡塔尔似乎已经暂
财商
供应“安全感”超过红海“危机感”?欧洲天然气价格大跌
虽然冬季极寒天气来临,而且卡塔尔似乎已经暂
财商

