和黄医药宣布沃瑞沙® (ORPATHYS®) 和泰瑞沙® (TAGRISSO®) 的联合疗法用于治疗伴有MET扩增的一线EGFR抑制剂治疗后疾病进展的肺癌患者的中国新药上市申请获受理并获纳入优先审评
 |
香港、上海和新泽西州弗洛勒姆公园2025年1月2日 /美通社/ -- 和黄医药(中国)有限公司(简称"和黄医药"或"HUTCHMED")(纳斯达克/伦敦证交所:HCM;香港交易所:13)今日宣布沃瑞沙®(ORPATHYS®,赛沃替尼/ savolitinib)和泰瑞沙®(TAGRISSO®,奥希替尼/ osimertinib)的联合疗法用于治疗伴有MET扩增的接受一线表皮生长因子受体("EGFR")抑制剂治疗后疾病进展的EGFR突变阳性局部晚期或转移性非小细胞肺癌患者的新药上市申请已获中国国家药品监督管理局("国家药监局")受理并予以优先审评。沃瑞沙®是一种强效、高选择性的口服MET 酪氨酸激酶抑制剂("TKI")。泰瑞沙®是一种不可逆的第三代EGFR TKI。此次受理也将触发一项来自阿斯利康的里程碑付款。
多中心、开放标签、随机对照的SACHI III期研究的数据支持了此项新药上市申请。该研究评估了泰瑞沙®与沃瑞沙®联合疗法对比当前此类疾病的标准疗法铂类双药化疗(培美曲塞加顺铂或卡铂)的疗效及安全性。研究的主要终点是研究者评估的无进展生存期("PFS")。其他终点包括独立监察委员会评估的PFS,总生存期(OS)、客观缓解率(ORR)、缓解持续时间(DoR)、疾病控制率(DCR)、到达疾病缓解的时间(TTR)及安全性。SACHI研究的独立数据监察委员会(IDMC)在预设的中期分析中认定该研究已达到预设的主要终点PFS,因此该研究的患者入组已停止。 SACHI研究的结果将提交于即将召开的学术会议发表(clinicaltrials.gov 注册号 NCT05015608)。
和黄医药研发负责人及首席医学官石明博士表示:"这是沃瑞沙®和泰瑞沙®联合疗法的首个监管注册申请。该联合疗法在解决 MET 驱动的 EGFR 抑制剂耐药问题方面已展示了明确的证据,并让延续口服用药成为可能。透过我们的生物标记物特异性方法,我们希望能够提高非小细胞肺癌患者的治疗连续性和生活质量,以应对这一充满挑战的旅程。我们以及合作伙伴阿斯利康正在全球范围内探索这种联合疗法,开展了一系列包括TATTON、SAVANNAH、SAFFRON 和ORCHARD 研究在内的后期临床试验。我们希望在不久的将来为患有MET驱动的肺癌患者带来这种全口服、免化疗的治疗选择。"
沃瑞沙®和泰瑞沙®联合疗法已于2024年12月获国家药监局纳入突破性治疗品种用于此潜在适应症。国家药监局将该联合疗法纳入突破性治疗品种,认可了其作为治疗严重疾病的新疗法,其临床证据表明较现有治疗手段的明显优势。
- 天府智算西南算力中心投运! 算效、能效创双高!
- 美国万通证券宣布完成其客户理臣中国313 万美元的注册直接发行(纳斯达克代码:LICN)
- SK启方半导体推出HVIC工艺技术,扩大高压代工服务组合
- 中荷人寿山东省分公司积极开展“金融教育宣传月”户外宣传活动
- Sirnaomics宣布完成针对靶向APOC3用于治疗心血管疾病的STP125G在非人灵长类动物模型中安全性和有效性的IND准备阶段研究
- 万千滋味同消夏,万豪中餐厅邀宾客以美味开启夏日序曲
- 媒体观察:40年创新蝶变,IBM 与中国共创新质生产力
- DAHON大行公路车Vélodon,轻驰出发,探索新世界
- "以我为名 为国而战"2024中国乒乓球队龙服揭晓
- 第五届“指尖上的智慧”珠算文化非遗教育成果展演启动仪式在京成功举办
- 舒华体育参建文昌航天运动中心 以专业力量助力中国航天梦
- 2024上海老博会6月盛启,共见银发经济新时代
- 曝光义乌市豪肥贸易有限公司成都分公司不断创新,不断发现新鲜元素
- Masdar签署协议,将开发1GW Mingbulak风电场
- IBM专家解读watsonx新功能: 硬币的两面
- 重塑消费信任,探索营销渠道 HNC健康营养展寻商会成功举办
- 匹克签约委内瑞拉篮协 持续加码国际篮球市场
- Global Bridge Associates宣布建立新的合作伙伴关系和网站,推动学生寄宿家庭业务拓展
- 加速5G普及,TCL 两款5G手机创新适老化智能体验
- 联合国开发计划署和IBM推出预测能源获取和能源公平性的新模型工具
推荐
-
 娃哈哈这艘商业巨舰将驶向何方,我们试目以待
2月25日,娃哈哈集团在官网发布讣告,娃哈哈创
财商
娃哈哈这艘商业巨舰将驶向何方,我们试目以待
2月25日,娃哈哈集团在官网发布讣告,娃哈哈创
财商
-
 春节将至,抢票再次成为广大网友关注的热门话题
春节将至,抢票再次成为广大网友关注的热门话
财商
春节将至,抢票再次成为广大网友关注的热门话题
春节将至,抢票再次成为广大网友关注的热门话
财商
-
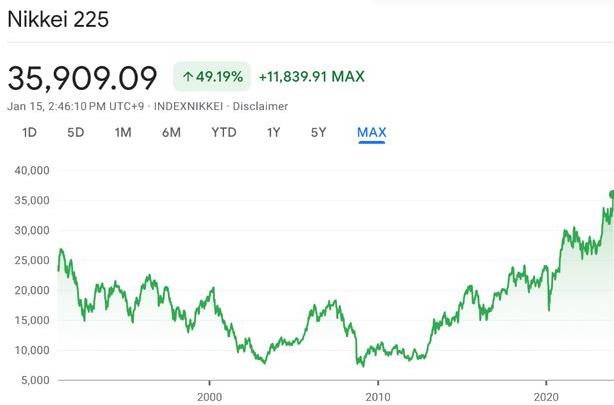 日股盘中再破34年新高,今年还涨得动吗?
今年日股开局强势,1月5日以来开启连涨行情,日
财商
日股盘中再破34年新高,今年还涨得动吗?
今年日股开局强势,1月5日以来开启连涨行情,日
财商
-
 广东省药监局调研恒昌医药集团,聚焦药品流通产业高质量发展
日前,广东省药品监督管理局党组成员、副
财商
广东省药监局调研恒昌医药集团,聚焦药品流通产业高质量发展
日前,广东省药品监督管理局党组成员、副
财商
-
 我们时常把创业想得太过简单,认为获得成功轻而易举
我们时常把创业想得太过简单,认为获得成功
财商
我们时常把创业想得太过简单,认为获得成功轻而易举
我们时常把创业想得太过简单,认为获得成功
财商
-
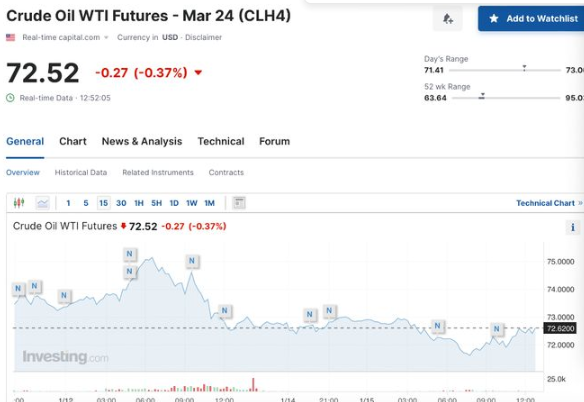 供应“安全感”超过红海“危机感”?欧洲天然气价格大跌
虽然冬季极寒天气来临,而且卡塔尔似乎已经暂
财商
供应“安全感”超过红海“危机感”?欧洲天然气价格大跌
虽然冬季极寒天气来临,而且卡塔尔似乎已经暂
财商
-
 为何娃哈哈纯净水线上会卖断货?
随着网络上关于娃哈哈和农夫山泉之争的持续
财商
为何娃哈哈纯净水线上会卖断货?
随着网络上关于娃哈哈和农夫山泉之争的持续
财商

