勃林格殷格翰nerandomilast 治疗进展性肺纤维化FIBRONEER™-ILD III期研究达到主要终点
- FIBRONEER™-ILD临床试验概要结果显示:与安慰剂相比,接受在研化合物nerandomilast治疗的第52周,患者的用力肺活量(mL)较基线的绝对变化达到主要终点
- FIBRONEER™-ILD是在研化合物nerandomilast第二个达到主要终点的III期试验[1]
- FIBRONEER™系列临床试验的初步安全性和耐受性结果与其特发性肺纤维化II期试验结果基本一致;FIBRONEER™-ILD临床试验的疗效和安全性完整数据将于2025年二季度公布
- 勃林格殷格翰将向美国食品药品监督管理局(FDA)及全球范围内的其他卫生监管机构递交nerandomilast用于治疗进展性肺纤维化(PPF)的新药申请
德国殷格翰2025年2月11日 /美通社/ -- 2025年2月10日,勃林格殷格翰宣布FIBRONEER™-ILD临床试验达到其主要终点,即与安慰剂相比,第52周时患者的用力肺活量(FVC,mL)较基线的绝对变化。FVC是衡量肺功能的指标。[2] FIBRONEER™系列试验的初步数据与其特发性肺纤维化(IPF)II期研究的安全性和耐受性数据基本一致,总体不良反应与安慰剂组相当。[3]
Nerandomilast是一款在研的口服选择性磷酸二酯酶4B(PDE4B)抑制剂,[3]目前尚未获批,因此安全性和有效性有待验证。目前正在开展FIBRONEER™全球研发项目,该项目包含两项III期临床研究:针对特发性肺纤维化(IPF)患者的FIBRONEER™-IPF研究[4],以及针对进展性肺纤维化(PPF)患者的FIBRONEER™-ILD[5]研究。
基于这些研究结果,勃林格殷格翰将向美国食品药品监督管理局(FDA)及全球范围内的其他卫生监管机构递交nerandomilast用于治疗PPF的新药申请。
勃林格殷格翰人用药品业务负责人、执行董事会成员Shashank Deshpande表示:"FIBRONEER™-ILD积极的研究结果显示了nerandomilast在治疗进展性肺纤维化上的潜力。我们希望目前初步的安全性和耐受性结果有望减少治疗挑战。FIBRONEER™临床试验项目的最新进展印证了我们致力于改善这种致衰性疾病患者生活质量的承诺,也彰显了勃林格殷格翰在肺纤维化研究领域的前沿地位。"
关于FIBRONEER™-ILD (NCT05321082) [5]
FIBRONEER™-ILD是一项双盲、随机、安慰剂对照试验,评估nerandomilast(BI 1015550)在PPF患者中至少治疗52周的疗效和安全性。
主要终点:基线至第52周的FVC(mL)的绝对变化。
关键次要终点:
- 试验期间首次发生以下任一复合终点事件的时间:首次出现急性ILD加重、首次因呼吸系统原因住院、或死亡(以先发生者为准)。
参与FIBRONEER™-ILD临床试验的患者,将接受至少52周内接受口服nerandomilast治疗,每日两次,剂量为9 毫克或18 毫克,或作为对照组接受安慰剂治疗。Nerandomilast每日两次,每次18毫克的剂量选择是基于II期临床试验的结果。[2]新增设的每日两次,每次9毫克的剂量,旨在评估较低剂量下的获益-风险情况,并提供进一步的剂量-效应及暴露-效应的数据。[2]
该临床试验已在40多个国家的400多个研究中心开展,并招募了1178名患者。
关于FIBRONEER™临床项目
FIBRONEER™项目包括两项III期随机、双盲、安慰剂对照试验:FIBRONEER™-IPF(NCT05321069)[4]和FIBRONEER™-ILD(NCT05321082)[5],旨在研究nerandomilast在IPF和PPF患者中治疗至少52周的疗效、安全性和耐受性。
两项研究中,主要终点均为第52周时FVC较基线水平的绝对变化。关键次要终点为试验期间首次发生以下任一复合终点事件的时间:首次出现IPF/PPF急性加重、首次因呼吸系统原因住院、或死亡(以先发生者为准)。
关于Nerandomilast
Nerandomilast(BI 1015550)是一款在研的口服磷酸二酯酶4B(PDE4B)抑制剂,正被开发作为特发性肺纤维化(IPF)和进展性肺纤维化(PPF)的潜在治疗药物。[3],[4],[5]该化合物目前仍处于研发阶段,尚未获批,其疗效和安全性也有待验证。
Nerandomilast于2022年2月获得美国食品药品监督管理局(FDA)授予的特发性肺纤维化(IPF)突破性疗法认定。[6]
一项针对147名IPF患者的II期随机、双盲、安慰剂对照临床试验,研究了nerandomilast的疗效、安全性及患者耐受性。[3]该研究的主要终点为12周治疗期间FVC(用力肺活量)相较于基线的变化水平。[3]
关于特发性肺纤维化(IPF)和进展性肺纤维化(PPF)
特发性肺纤维化(IPF)是一类较为常见的进行性纤维化间质性肺疾病(ILD)。[7]其临床症状包括:活动诱发的呼吸急促、持续干咳、胸部不适、疲劳和乏力。尽管被视为"罕见"病,但IPF影响了全球约三百万人。[8]该疾病主要影响50岁以上的人群,且男性患者多于女性。[8]
患有某些非特发性肺纤维化 (IPF) 类型的 ILD 患者也可能出现进行性表型,称为进展性肺纤维化(PPF)。除特发性肺纤维化(IPF)以外的其他间质性肺疾病(ILD)中,进展性肺纤维化的定义为呼吸症状加重、生理监测中可观察到疾病恶化,以及影像学检查结果所证实的疾病进展。[9]
[1] Boehringer Ingelheim (2024) Boehringer's nerandomilast meets primary endpoint in pivotal phase-III FIBRONEER™-IPF study. Accessed January 2025. Available at: https://www.boehringer-ingelheim.com/us/topline-results-boehringers-phase-iii-ipf-study
[2] Maher TM, et al. (2023) Design of a phase III, double-blind, randomised, placebo-controlled trial of BI 1015550 in patients with progressive pulmonary fibrosis (FIBRONEER-ILD). In: BMJ Open Respir Res 2023;10:e001580.
[3] Richeldi L, et al. (2022) Trial of a Preferential Phosphodiesterase 4B Inhibitor for Idiopathic Pulmonary Fibrosis. In: N Engl J Med 2022;386:2178-2187.
[4] Boehringer Ingelheim (2024) A Study to Find Out Whether BI 1015550 Improves Lung Function in People With Idiopathic Pulmonary Fibrosis (IPF). Accessed January 2025. Available at: https://clinicaltrials.gov/study/NCT05321069
[5] Boehringer Ingelheim (2024) A Study to Find Out Whether BI 1015550 Improves Lung Function in People With Progressive Fibrosing Interstitial Lung Diseases (PF-ILDs). Accessed January 2025. Available at: https://clinicaltrials.gov/study/NCT05321082?tab=results.
[6] Boehringer Ingelheim (2022) FDA Grants BI 1015550 Breakthrough Therapy Designation for Idiopathic Pulmonary Fibrosis. Accessed January 2025. Available at: https://www.boehringer-ingelheim.com/us/human-health/lung-diseases/pulmonary-fibrosis/fda-grants-bi-1015550-breakthrough-therapy.
[7] Sauleda J, et al. Idiopathic Pulmonary Fibrosis: Epidemiology, Natural History, Phenotypes. Med Sci (Basel). 2018 Nov 29;6(4):110. doi: 10.3390/medsci6040110. PMID: 30501130; PMCID: PMC6313500.
[8] Koudstaal T, et al. (2023) Idiopathic pulmonary fibrosis. In: Presse Med 2023; 52(3):104166
[9] Cottin, V. et al. (2023) Criteria for Progressive Pulmonary Fibrosis: Getting the Horse Ready for the Cart. In: Am J Respir Crit Care Med 2023; 207(1):11-13
关于勃林格殷格翰
勃林格殷格翰是全球领先的生物制药企业,布局人用药品、动物保健两大业务领域。公司研发投入位居行业前列,致力于研究突破性疗法,解决巨大未满足的医疗需求,从而帮助改善或延长生命。自1885年成立以来,勃林格殷格翰一直是独立的家族企业,始终着眼长远发展,将可持续发展理念贯穿全价值链。公司在全球有超过5.35万名员工,服务逾130个市场,致力于打造一个更健康、更可持续、更公平的未来。更多详情,请访问:www.boehringer-ingelheim.cn, www.boehringer-ingelheim.com
- Cell Impact已收到电解领域价值1800万瑞典克朗的订单
- 郑石轩:践行高质量发展,粤海以更优产品力推动水产业变革
- Colt DCS 计划在伦敦西部海斯(Hayes)购买土地以扩建超大规模数据中心
- 宝马宣布增加在华投资200亿,全力以赴迎接"新世代"国产
- 国庆夜游正当时,万豪旅享家邀宾客旅途中遍赏华灯璀璨
- 繁华之上 五载艺韵:品鉴"柏"味,雅宅"悦"享
- Automation Anywhere与Microsoft合作,通过集成企业自动化和Microsoft Azure OpenAI服务,将自动化变为可能
- 原生态与匠心并行,高端创意品牌集Uniche空降中国进博会
- 疆果果创始人陈文君:新疆“大坚果专家”,要成为“大”,离不开“精”
- 凯悦酒店集团增长势头持续,全球筹备中酒店客房数达129,000间,创历史新高
- 无限极获批国家级联合实验室项目,开启中国与欧洲科研合作新篇章
- Enjoy Scent隐迹香氛·微光公益再出发
- 从XR光学到车载HUD:歌尔光学CIOE 2024勾勒智能视界新蓝图
- 亚马逊云科技发布Amazon Q Developer新功能,加速大规模传统工作负载的转型
- COP29|中国企业气候行动案例集发布,彰显企业气候责任
- 第136届广交会推出全新移动APP,旨在提升参会体验
- 汤普金斯自然保护组织将档案存放在斯坦福大学图书馆,旨在支持智利和阿根廷持续进行的实地调研
- 「澳門銀河」诠释奢华身心健康美学
- 帝斯曼-芬美意参展2024年中国(国际)乳业技术博览会
- WEXIT :富有的英国人提前退出欧盟
- 协鑫集团应邀出席江苏--非洲经贸合作交流会
- 博奥信宣布与Aclaris Therapeutics就两项潜在的同类首创和同类最佳免疫药物资产达成全球独家授权许可协议
- 义诊进楼宇 情暖和乔
- 新质青年,蓄势正发丨2024中国(广东)大学生时装周圆满闭幕
- 沃特世推出新型生物分离工具,利用 LC-MS 分析技术加快并改进RNA疫苗和治疗药物开发
- 第九届 Morketing Summit 灵眸大赏圆满闭幕
- 陈天桥雒芊芊脑科学研究院OMNE人工智能长期记忆框架荣登GAIA排行榜榜首
- 粤海饲料专家聚首谋发展,董事长郑石轩解读最新战略构想
- 小菜园登陆港交所,大众便民中式正餐现代化开启新篇章
- 甲旁减疗法创新有望助力患者摆脱传统治疗困境
推荐
-
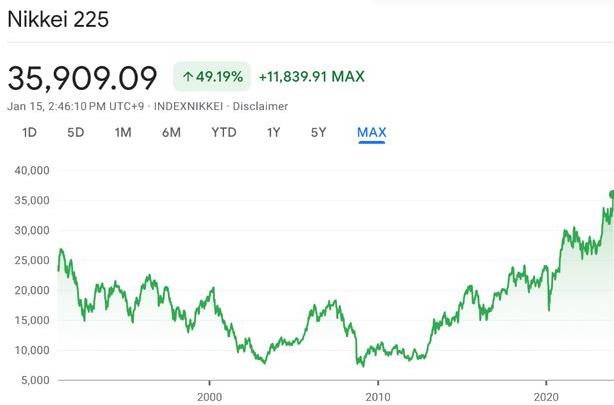 日股盘中再破34年新高,今年还涨得动吗?
今年日股开局强势,1月5日以来开启连涨行情,日
财商
日股盘中再破34年新高,今年还涨得动吗?
今年日股开局强势,1月5日以来开启连涨行情,日
财商
-
 为何娃哈哈纯净水线上会卖断货?
随着网络上关于娃哈哈和农夫山泉之争的持续
财商
为何娃哈哈纯净水线上会卖断货?
随着网络上关于娃哈哈和农夫山泉之争的持续
财商
-
 我们时常把创业想得太过简单,认为获得成功轻而易举
我们时常把创业想得太过简单,认为获得成功
财商
我们时常把创业想得太过简单,认为获得成功轻而易举
我们时常把创业想得太过简单,认为获得成功
财商
-
 春节将至,抢票再次成为广大网友关注的热门话题
春节将至,抢票再次成为广大网友关注的热门话
财商
春节将至,抢票再次成为广大网友关注的热门话题
春节将至,抢票再次成为广大网友关注的热门话
财商
-
 广东省药监局调研恒昌医药集团,聚焦药品流通产业高质量发展
日前,广东省药品监督管理局党组成员、副
财商
广东省药监局调研恒昌医药集团,聚焦药品流通产业高质量发展
日前,广东省药品监督管理局党组成员、副
财商
-
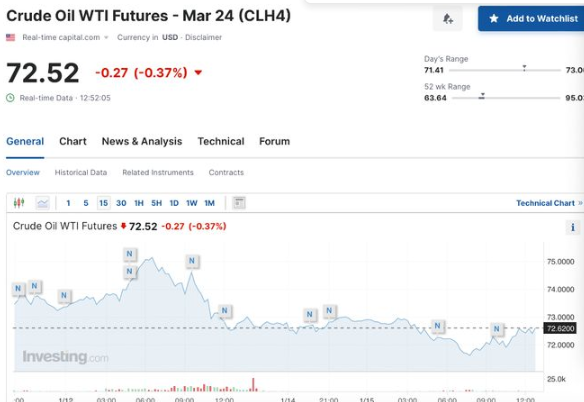 供应“安全感”超过红海“危机感”?欧洲天然气价格大跌
虽然冬季极寒天气来临,而且卡塔尔似乎已经暂
财商
供应“安全感”超过红海“危机感”?欧洲天然气价格大跌
虽然冬季极寒天气来临,而且卡塔尔似乎已经暂
财商
-
 娃哈哈这艘商业巨舰将驶向何方,我们试目以待
2月25日,娃哈哈集团在官网发布讣告,娃哈哈创
财商
娃哈哈这艘商业巨舰将驶向何方,我们试目以待
2月25日,娃哈哈集团在官网发布讣告,娃哈哈创
财商

